Dr. Gustavo Freier (Sanatorio San Carlos), Dr. Agustín Dal Verme (Hospital Zonal de Esquel), Dra. Julia Muzio (Intecnus), Dra. Andreina Danti (Hospital Sub-Zonal de Rawson), Dr. Abel G. Ojeda (Hospital Zonal de San Martin de los Andes)
Un hombre de 59 años con antecedentes de ACV isquémico, artritis psoriatica en tratamiento con Ustekinumab, reemplazo total de rodilla izquierda y epilepsia, consulta en el Servicio de Guardia por dolor abdominal en epigastrio de 12 hs de evolución. La intensidad del dolor es 10/10 y se irradia a tórax y espalda. Estuvo internado en reiteradas oportunidades en el último año por episodios similares. No tuvo fiebre, escalofríos, hematemesis, diarrea, melena, hematoquecia, no toma anti-inflamatorios no esteroideos, no consume alcohol.
Al ingreso presentaba una frecuencia cardiaca de 93 x’. una tensión arterial de 128/82, frecuencia respiratoria de 18 x’, temperatura axilar de 36.5°C y la Saturación de oxigeno era del 100% respirando aire ambiente.
Al examen físico presentaba signos compatibles con la presencia de líquido intrabdominal, onda ascítica y matidez que se modifica con los cambios de decúbito. Los ruidos hirdoaéreos eran normales, presentaba dolor en epigastrio, línea media abdominal e hipocondrio izquierdo sin defensa ni reacción peritoneal.
Laboratorio:

Electrocardiograma: Ritmo sinusal, intervalo PR prolongado
No muestra cambios en el segmento ST.
Frente a una persona con múltiples factores de riesgo para enfermedad cardiovascular, antecedentes de enfermedad autoinmune y dolor abdominal recurrente nos planteamos los siguientes diagnósticos diferenciales:
- Síndrome coronario agudo.
- Cólico Biliar.
- Pancreatitis aguda
- Ulcera péptica.
- Peritonitis bacteriana espontanea.
Consideramos que es muy importante priorizar aquellas situaciones clínicas que le pueden comprometer la vida como un síndrome coronario agudo, pero nuestro paciente con factores de riesgo y dolor de 12 hs de evolución, no presentaba cambios electrocardiográficos lo cual nos hizo descartar esta posibilidad.
El cólico biliar generalmente es un dolor de comienzo súbito se irradia al hombro derecho, es intermitente y su duración es de 1 a 5 horas. La localización del dolor no es típica al igual que la duración del dolor demasiado prolongado descartando asi esta posibilidad.
La pancreatitis aguda es de diagnóstico clinico ante la presencia de 2 de las siguientes 3 características, dolor epigástrico severa, amilasa o lipasa 3 veces superior al límite superior normal e imágenes radiológicas compatibles con pancreatitis aguda. En base al dolor epigástrico y el valor de lipasa confirmamos el diagnostico de pancreatitis aguda.
La ulcera péptica se presenta en personas con factores de riesgo como el consumo de antinflamatorios no esteroides o abuso de alcohol con síntomas digestivos altos como acidez y/o nauseas, consideramos esta opción poco probable.
La peritonitis bacteriana espontanea podría considerarse por la distensión y dolor abdominal, pero faltaban signos de infección aguda y fiebre.
El paciente fue internado para reposición de volumen parenteral y analgesia EV.
Al preguntar sobre mas antecedentes nos refirió la persistencia de la distención abdominal a pesar de haber tenido múltiples paracentesis.
Se realiza una ecografía abdominal donde no se observó litiasis vesicular ni dilatación de la vía biliar.
Si bien las imágenes no son necesarias para el diagnóstico o manejo inicial de la pancreatitis aguda ante estos hallazgos decidimos realizar una tomografía computada de abdomen y pelvis con contraste EV ya para evaluar la posibilidad de colecciones liquidas, masas, necrosis, litiasis, calcificaciones o posibles hemorragias, En la misma se visualizó una dilatación del conducto pancreático con una imagen litiasis de 4 mm a nivel de la parte proximal del cuerpo pancreático, edema peripancreático, ascitis moderada y 3 colecciones liquidas peripancreáticas que sugieren una pancreatitis aguda sobre una pancreatitis crónica.
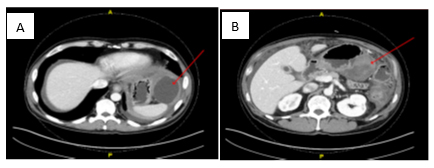
Como observamos en las imágenes observamos una imagen (B) de contenido heterogéneo encapsulada de 7.0 x 4.9 cm a lo largo del cuerpo del estómago, otra imagen (A) encapsulada de contenido liquido homogéneo en contacto con la cola del páncreas de 6.9 x 5.2 cm y una colección de líquido homogéneo de 1.3 cm en contacto con la parte posterior del bazo.
El manejo de las colecciones liquidas peripancreáticas pueden cambiar de acuerdo a sus características. La clasificación revisada de Atlanta para colecciones peripancreáticas está basada en las características morfológicas que se visualizan en la tomografía computada, las colecciones agudas son aquellas de contenido homogéneo sin necrosis ni pared y tienen menos de 4 semanas de evolución. Después de 4 semanas pueden tener pared epitelial y se refieren a los pseudoquistes pancreáticos. Las colecciones necróticas agudas están formadas por un contenido heterogéneo producto de material necrótico en proceso de licuefacción, no tienen pared y se encuentran durante las primeras 4 semanas, después de este periodo se forma una pared epitelial a su alrededor y se conocen como necrosis aislada.
Nuestro paciente tiene 2 imágenes compatibles con pseudoquistes y 1 compatible con necrosis aislada.
Él paciente ya tenía múltiples paracentesis de líquido ascítico y nuevamente se presenta con ascitis razón por la cual le repetimos nuevamente otra. El líquido abdominal era de color amarillo claro con 398 células nucleadas, 342 glóbulos blancos (<500) y 100 neutrófilos (<250), la concentración de amilasa era de 10880 U/L y lipasa 39780 U/L, la concentración de proteínas totales de 3.2 g/dl y 1.7 g/dl de albumina con una concentración sérica de albumina de 2.5 g/dl. El gradiente de albumina sérica y ascítica (GASA) de 0.8 g/dl.
En este momento no planteamos las siguientes etiologías probables de su ascitis recurrente.
- Fistula pancreática.
- Cirrosis no alcohólica.
- Insuficiencia Cardiaca.
- Secundaria a su medicación (Ustekinumab)
- Iatrogénica.
Debido a las características del líquido con una elevada concentración de amilasa y lipasa, una concentración de proteínas > 2.5 g/dl y una GASA <1.1 nos permite confirmar el diagnóstico de ascitis pancreática y nos permite diferenciarlo de otras causas.
La cirrosis no alcohólica presenta una GASA >1.1 y una concentración de proteínas < 2.5 g/dl.
La insuficiencia cardiaca presenta un GASA > 1.1 y una concentración de proteínas > 2.5 g/dl.
El Ustekinumab es una causa poco frecuente de pancreatitis aguda pero no explica la etiología de las colecciones.
El paciente no ha tenido intervenciones recientes como para explicar la causa iatrogénica, motivo por el cual lo descartamos.
En base al diagnóstico clinico de fistula pancreática por la recurrencia de las pancreatitis que evoluciona con colecciones recurrentes y persistentes más la aparición de nuevos pseudoquistes que es la manifestación más frecuente de las fistulas y la presencia de ascitis nos refuerza el diagnostico.
Consideramos que la conducta más apropiada era realizar una colangiografia por resonancia magnética en la que se observó un cálculo de 4 mm en el conducto pancreático a nivel del cuerpo con dilatación leve del conducto por detrás del cálculo en cuerpo y cola más una disrupción del mismo. El trayecto fistuloso se extiende hasta las colecciones, hallazgo que nos confirma el diagnóstico de fistula pancreática secundaria a la obstrucción del conducto por una calculo.
En base a este diagnóstico nos cuestionamos cual sería la conducta más apropiada para el manejo de nuestro paciente:
- Litotricia extracorpórea para romper el cálculo del conducto pancreático.
- Iniciar nutrición parenteral.
- Resección pancreática en el sitio de la fistula
- Seguimiento seriado con imágenes
- CEPRE con papilotomía, extracción del cálculo y colocación de un stent en el conducto pancreático.
La litotricia es un procedimiento a través del cual con ondas de choque y está indicado en cálculos mayores de 5 mm en los que no se puede realizar extracción endoscópica.
La nutrición enteral con sonda nasogástrica colocada por debajo de la 2da porción del duodeno demostró ser más efectiva que la nutrición parenteral en la pancreatitis aguda para el soporte nutricional en caso de que sea necesario.
La resección pancreática se considera un procedimiento de salvataje en caso de que persista la fistula a pesar de la intervención endoscópica.
El seguimiento con imágenes es útil para el seguimiento de lesiones o tumores, pero no es el indicado en esta situación.
La CEPRE es el procedimiento más indicado en esta situación cuando el manejo conservador ha fracasado.
Se le realizo la papilotomía, extracción del cálculo y colocación del stent con la consecuente mejoría de los síntomas y resolución de la fistula.
Comentarios:
La pancreatitis aguda es una de las causas más frecuentes de internación y ante su recurrencia debe sospecharse la presencia de una fistula debido a que la injuria crónica puede dañar el conducto pancreático.
La secreción exocrina del páncreas puede producir 1 litro de líquido por día, el cual puede generar una importante acumulación intrabdominal del mismo si el conducto excretor está dañado.
Los médicos debemos tener conciencia de los daños que puede producir una fistula pancreática y el desafío que nos genera llegar a su diagnóstico.
La ascitis pancreática se diagnostica ante la presencia de un exudado con una concentración de proteínas > 2,5 g/dl y un valor de amilasa > 1000 U/L.
La colangiografía por resonancia magnética es el estudio de elección para confirmar la presencia de una fistula pancreática.
El tratamiento conservador con reposición de líquidos EV y manejo del dolor sigue siendo la primera elección. Ante la persistencia del dolor y la acumulación de líquido debe considerarse el tratamiento endoscópico con colocación de stent. La operación de salvataje debe considerarse únicamente después del fracaso endoscópico y la persistencia de los síntomas. La cirugía tiene una mortalidad del 20% y un índice de recurrencia del 15%.
Referencias:
Larsen M, Kozarek R. Management of pancreatic ductal leaks and fistulae. J Gastroenterol Hepatol. 2014;29(7):1360-1370.
Tandan M, Reddy DN. Extracorporeal shock wave lithotripsy for pancreatic and large common bile duct stones. World J Gastroenterol.2011;17(39):4365-4371.
Al-Omran M, Albalawi ZH, Tashkandi MF, Al-Ansary LA. Enteralversus parenteral nutrition for acute pancreatitis. Cochrane Database Syst Rev. 2010;2010(1):CD002837.
Brun A, Agarwal N, Pitchumoni CS. Fluid collections in and around the pancreas in acute pancreatitis. J Clin Gastroenterol.2011;45(7):614-625.
